Hyperactieve Zeepaarden
Het lijkt een logische gedachte: als ons geheugen ons in de steek laat, zoals bij de ziekte van Alzheimer, dan zouden we dat toch ergens in het brein moeten kunnen meten in de vorm van veranderde hersenactiviteit? Een gebied dat stilgevallen is, of zich raar gedraagt? We kunnen inderdaad van alles meten aan de hersenen, met steeds meer detail, maar om dit nauwkeurig te doen op een patiëntvriendelijke manier is nog een uitdaging. De methoden om dit te doen worden gelukkig wel steeds beter, en de net gepubliceerde studie van onze promovendus Janne Luppi test een nieuwe aanpak om vroege afwijkingen op te sporen [1].
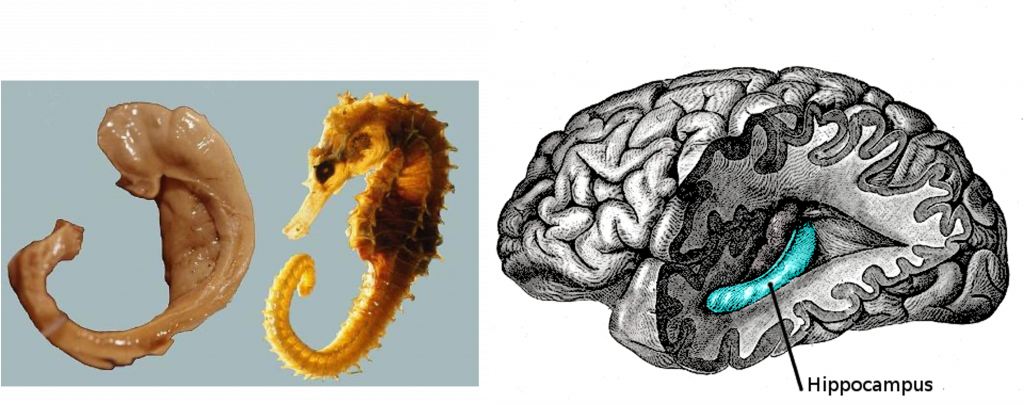
Aan de binnenkant van onze slaapkwabben ligt de hippocampus (Latijn voor zeepaard, vanwege de anatomische vorm van het gebied, zie figuur 1), een gebied dat heel belangrijk is voor ons geheugen, en dat vaak vroeg in de ziekte van Alzheimer al aangedaan is. Er stapelen eiwitten op, en er gaan hersencellen verloren. Een relatief nieuw inzicht is dat die hersencellen zich in een vroeg stadium ook anders gaan gedragen. Je zou misschien verwachten dat ze vertragen of helemaal stoppen met werken, maar in het begin lijkt er juist het tegenovergestelde te gebeuren: ze slaan op hol! Dit weten we vooral uit dierexperimenteel onderzoek, zoals in speciale muizen die ook de Alzheimerschade in hun hersenen vertonen, en waarbij er rechtstreeks in de hippocampus gemeten kan worden.
Chronisch overwerken is niet gezond
Sommige wetenschappers interpreteren de verhoogde activiteit als het compenseren voor schade: er zijn steeds minder goedwerkende cellen, dus degenen die overblijven, moeten harder hun best doen. Op zich een begrijpelijke gedachte, maar het lijkt toch anders te zitten: ten eerste is het niet logisch dat beschadigde hersencellen minder hard gaan vuren. Het kost ze juist relatief veel energie om niet te vuren, dus als de energieaanvoer stokt, valt de rem weg, en kan een neuron (hersencel) op hol slaan.
Ten tweede: dat snellere vuren is niet zinvol, want hersencellen kunnen het best met elkaar communiceren als ze hun vuursnelheid flexibel op elkaar kunnen afstemmen, en dat betekent soms vertragen, en soms versnellen. Een cel die alleen maar sneller gaat vuren verliest veel energie, en kan niet meer zinvol communiceren met zijn omgeving. Het is dus geen zinvolle overactiviteit, maar pathologische. En zij zal de hersencel uiteindelijk uitputten en ten gronde richten.
Tegelijk hyperactiviteit en vertraging: een paradox?
Zien we dan op een EEG- of MEG-meting [2], die van buitenaf hersenactiviteit registreren, deze gebieden van hyperactiviteit terug? Tot nu toe was het antwoord: nee. We zien het tegenovergestelde; bij de ziekte van Alzheimer vertragen hersenritmes juist geleidelijk, dit is al decennia bekend. Hoe kan dit? Vanwaar deze tegenstrijdige bevindingen? Het antwoord hierop is het gigantische schaalverschil waar we over praten: EEG en MEG meten de hersenactiviteit van miljoenen hersencellen tegelijk. Het signaal dat we opvangen is niet het vuurgedrag van afzonderlijke cellen, maar een grote optelsom van de activiteit in een gebied (van een paar milli-/centimeter). Uit dit signaal is niet goed het gedrag van individuele cellen te herleiden, maar we weten wel van experimenten met computermodellen, zoals van promovenda Anne van Nifterick (hierover binnenkort meer) dat hyperactiviteit op celniveau juist heel goed kan leiden tot vertraging op grote schaal. Dit voelt erg onwaarschijnlijk, maar is wel verklaarbaar: voor de sneller vurende neuronen is het erg moeilijk geworden om hun activiteit op elkaar af te stemmen, en zo elkaar dus te versterken. Dit is nodig om in het EEG/MEG signaal zichtbaar tevoorschijn te komen. Lukt dat niet, dan resteert netto vooral de langzame activiteit. Helaas is deze vertraging in de vroege fase van de ziekte vaak nog niet zo duidelijk, en is het een te ongevoelige test om de ziekte in een vroeg stadium op te sporen bij individuen.
Focus op de hippocampus
Bij patiënten zagen we tot nu toe dus eigenlijk vooral geleidelijk vertragende hersenactiviteit. Tenminste, als je vooral naar de buitenste schors van de hersenen kijkt. Met MEG is het echter mogelijk om beter naar dieper gelegen gebieden te kijken, zoals de hippocampus. Onze onderzoeksvraag was daarom: laat de hippocampus in een vroeg stadium van Alzheimer misschien abnormale activiteit zien, waarmee we de ziekte vroeger en specifieker kunnen aantonen? Het voorlopige antwoord lijkt bevestigend: als we kijken naar activiteit in verschillende gebieden, dan zien we dat de hippocampi (en vooral de rechter) zich apart gedragen: er is meer activiteit ten opzichte van dezelfde gebieden in de controlegroep, en ook ten opzichte van andere hersengebieden in dezelfde groep. Er is sprake van vertraging, maar ook juist wat meer relatief snelle ‘alfa’ activiteit (zie figuur 2). Dit zou een teken kunnen zijn dat we iets specifieks oppikken…
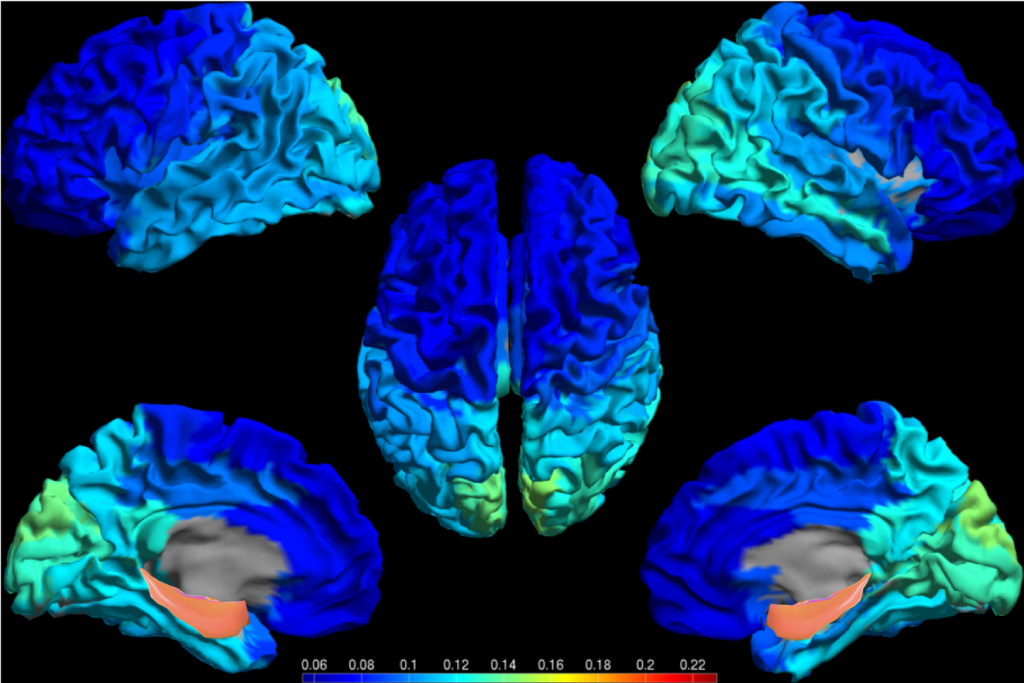
Figuur 2. Projecties van hersenactiviteit in verschillende hersengebieden. Patiënten in de vroege fase van Alzheimer laten relatief veel alfa activiteit (8-13 Hz) zien, en dit is vooral het geval in de hippocampus beiderzijds (in rood weergegeven).
Voorspelt ontregelde hippocampusactiviteit alzheimer?
Uiteindelijk is het van belang dat we niet alleen tussen groepen verschillen vinden, maar op individueel niveau. Om te zien of we op basis van de abnormale activiteit in de hippocampi een goed onderscheid kunnen maken tussen vroege Alzheimerpatiënten versus gezonde mensen, keken we of de hippocampusactiviteit kon voorspellen in welke groep iemand hoort. En wat bleek: de rechter hippocampus was de beste voorspeller! Niet perfect, maar wel beter dan de gebieden in de hersenschors waar we normaal naar kijken.
Wat is het belang van deze bevindingen?
Het vinden van abnormale hippocampus activiteit in dit vroege stadium van de ziekte van Alzheimer (waarin mensen wel geheugenklachten hebben, maar nog geen dementie hebben, en zelfstandig functioneren) is een mooi resultaat. Er is nog meer onderzoek nodig om te kijken of het nog beter kan, en of deze bevinding specifiek is voor de ziekte van Alzheimer. Ook kunnen we niet hard maken dat de afwijkende hippocampusactiviteit een uiting van onderliggende hyperactiviteit (op celniveau) is, omdat we op (veel) te grof niveau kijken. Al is dit wel een logische veronderstelling. Hoe dan ook, ongeacht het onderliggend mechanisme, als deze bevinding specifiek is voor Alzheimer, zou het een elegante methode kunnen worden om in een vroeg stadium de ziekte te detecteren. Dit is tegenwoordig van groot belang voor studies met nieuwe Alzheimer medicatie. Daarnaast zou de hyperactiviteit zelf een aangrijpingspunt kunnen zijn voor nieuwe therapieën; het beïnvloeden van hersenactiviteit is in opkomst, en wij houden ons hier ook mee bezig, zoals met het ExMachina project [3]. Wordt vervolgd!
Referenties
[1] Luppi, J. J., Schoonhoven, D. N., van Nifterick, A. M., Gouw, A. A., Hillebrand, A., Scheltens, P., … & de Haan, W. (2022). Oscillatory Activity of the Hippocampus in Prodromal Alzheimer’s Disease: A Source-Space Magnetoencephalography Study. Journal of Alzheimer’s Disease, (Preprint), 1-17.
[2] www.alzheimercentrum.nl/blogartikel/wat-is-knf
[3] www.alzheimercentrum.nl/blogartikel/het-exmachina-project